1. 抗原、抗体
▌概念及应用
抗原:指能引起抗体生成的物质,是任何可诱发免疫反应的物质。
抗体:机体在抗原物质刺激下,由B细胞分化成的浆细胞所产生的、可与相应抗原发生特异性结合反应的免疫球蛋白。
▌抗原的制备
根据抗原来源的不同,可分为天然蛋白质抗原、基因重组抗原、合成性抗原和小分子半抗原。
抗原通用特点:
分子量大:大分子物质能长时间留在机体内,有更多机会和免疫细胞(主要是巨噬细胞、T淋巴细胞和B淋巴细胞)接触,引起免疫细胞作出免疫反应。
外源性强:个体形成的早期,机体对自身物质形成免疫耐受,与机体物质相似度很高的物质一般不会引起机体产生免疫反应,只有异质性的物质侵入体内,机体才能迅速对抗外来物质的侵害,保护自身。
结构复杂:外源性只是从归类宏观角度上论述抗原性问题,实际上从微观上来说,作为抗原的分子物质的结构必须尽可能复杂,简单重复的序列或者直链物质(比如:糖、氨基酸)组成的序列一般抗原性都很弱。
降解性好:作为抗原,必须是可以降解才能抗原提呈。

▌抗体的制备
根据制备的原理和方法可分为多克隆抗体、单克隆抗体及基因工程抗体三类。


1) 多克隆抗体
早年人工制备抗体的方法主要是以相应抗原免疫动物,获得抗血清。由于天然抗原常含多种不同抗原表位,在含多种抗原表位的抗原物质刺激下,体内多个B细胞克隆被激活并产生针对多种不同抗原表位的抗体,其混合物即为多克隆抗体。
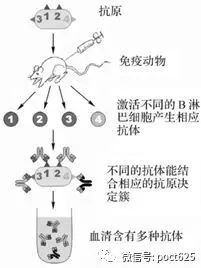
多克隆抗体是机体发挥特异性体液免疫效应的关键分子,具有中和抗原、免疫调理、介导CDC、ADCC等重要作用。在体外,多克隆抗体主要来源于动物免疫血清、恢复期病人血清或免疫接种人群。其特点是来源广泛、制备容易。多克隆抗体是针对不同抗原表位的抗体的混合物,而并非仅针对某一特定表位,其缺点是:特异性不高、易发生交叉反应,也不易大量制备,从而应用受限。
2)单克隆抗体
单克隆抗体是由单一B细胞克隆产生的高度均一、仅针对某一特定抗原表位的抗体。
制备单一表位特异性抗体的理想方法是获得仅针对单一表位的浆细胞克隆,使其在体外扩增并分泌抗体。然而,浆细胞在体外的寿命较短,也难以培养。故可产生特异性抗体但短寿的浆细胞与无抗原特异性但长寿的恶性浆细胞瘤细胞融合,建立可产生单克隆抗体的杂交瘤技术。
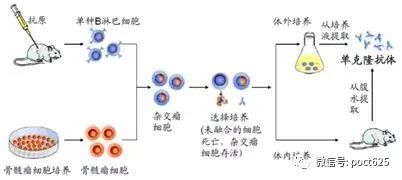
单克隆抗体在结构和组成上高度均一,抗原特异性及同种型一致,易于体外大量制备和纯化。因此,其具有纯度高、特异性强、效价高、少或无血清交叉反应、制备成本低等优点,已广泛用于疾病诊断、特异性抗原或蛋白的检测和鉴定、疾病的被动免疫治疗和生物导向药物制备等。
3) 基因工程抗体
也被称作重组抗体。是使用重组DNA技术在体外构建的,不受免疫系统限制而生产的单克隆抗体。是利用重组DNA及蛋白质工程技术对编码抗体的基因按不同需要进行加工改造和重新装配,经转染适当的受体细胞所表达的抗体分子。
生物学原理:
从生物学原理的角度看,只要分离出抗体基因,然后并入质粒DNA载体中,将得到的合成质粒转移到表达宿主,如细菌、酵母或哺乳动物细胞系中,即可在体外表达得到重组抗体,进一步经过分离纯化,变成了高效纯化的重组抗体。一般而言,但凡单克隆抗体适用的场合,重组抗体也完全适用。
基因工程抗体五大种类:
嵌合抗体、人源性抗体、完全人源化抗体、单链抗体、双特异性抗体。
基因工程抗体与单克隆抗体相比的优势:
通过基因工程技术的改造,可降低甚至消除人体对抗体的排斥反应;
基因工程抗体的分子量较小,可部分降低抗体的鼠源性,更加有利于穿透血管壁,进入病灶的核心部位;
可采用原核细胞、真核细胞和植物等多种表达方式,大量表达抗体分子,大大降低生产成本。
2. 行业痛点
原来都是代理商代理国外品牌,起步晚,工艺要求高,技术滞后。而原料的研发周期长、技术壁垒高,从而阻碍国内企业从根本上改善试剂质量。因此,目前国内厂家只能采取自主研发或对外合作的方式开发原材料,或者通过优化生产工艺和研发思路来提升试剂质量,导至上游原料生产技术薄弱。
3.体外诊断酶
1) 概念
酶(enzyme)是由活细胞产生的、对其底物具有高度特异性和高度催化效能的蛋白质(多数)或RNA(少数),是一类极为重要的生物催化剂。
2) 作用机制
酶能显著地降低活化能,故能表现为高度的催化效率。

3)酶的来源
酶的生产工艺是决定其质量和产率的关键因素,力求选育高产菌株(包括构建基因工程菌),探索最优化的发酵工艺和后提取纯化技术,以提高酶的产率,保证原酶质量。
4. 发展趋势
通过诱变技术和底物诱导作用等方法,选育出稳定、高产的优良菌株是决定微生物发酵工程成败的关键所在。
寻找产生胞外酶的菌种,能为酶的提取纯化(下游工程)提供极大的便利。因为胞内酶分离中遇到大量菌体蛋白的干扰,使分离纯化程序复杂化,加大了目的酶的损失。而胞外酶无需破碎细菌细胞,培养液中杂蛋白量少,可用较为简捷的分离纯化方法加以提纯。
对传统的酶分离纯化工艺进行改进,采用温和、高效的生化新技术:如超滤技术、疏水层析技术等,能够显著提高目的酶的纯度和产率。
深化酶理化特性的研究,为诊断试剂配制中正确使用工具酶提供科学依据。
开辟工具酶的新用途,建立新的临床化学酶分析方法,以代替准确性和精密度均较差的化学方法,是一项很有意义的技术创新。
5.构建诊断试剂工具酶基因工程菌
细胞培养基
1) 概念
细胞培养基既是培养细胞中供给细胞营养和促使细胞生殖增殖的基础物质,也是培养细胞生长和繁殖的生存环境。体外培养的细胞直接生活在培养基中,因此培养基应能满足细胞对营养成分、促生长因子、激素、渗透压、pH等诸多方面的要求。
2)培养基的分类
细胞培养基经历血清、基础培养基、无血清培养基发展阶段。无血清细胞培养基提高了细胞表达蛋白的产量和质量,可简化分离、纯化及检测工艺,降低生产成本,适用于CHO细胞、杂交瘤细胞、骨髓瘤细胞及BHK细胞等,是最适合于生物药生产的培养基。无血清培养基也是抗体及重组蛋白生产的主要细胞培养基。
3)无血清培养基的优缺点分析
优点:
可避免血清批次间的质量变动,提高细胞培养和实验结果的重复性。
避免血清对细胞的毒性作用和血清源性污染。
避免血清组分对实验研究的影响。
有利于体外培养细胞的分化。
可提高产品的表达水平并使细胞产品易于纯化。
缺点:
细胞在无血清培养基中易受某些机械因素和化学因素的影响,培养基的保存和应用不如传统的合成培养基方便。
成本较高。
针对性很强,一种无血清培养基仅适合某一类细胞的培养。
无血清培养基行业特点:
A 无血清培养基开发技术壁垒高。由于细胞株的生物多样性,无血清培养基开发需要丰富的经验,Know-how处于首要位置,还需要大量实验筛选最合适的配方,并且不一定能够成功。无血清培养基涉及数十种原料的配比,每个产品的配方设计如何使得细胞密度更高、蛋白表达更多、产品稳定性更强,是企业产品的核心竞争力。
B 无血清培养基客户粘性强,客户更换供应商成本高。产品的研发一旦采用某种培养基,为了保持产品的稳定性,后续的实验方案、产品申报和上市生产将不能随意更改培养基品种,否则应重新注册申报。因此,企业产品研发和注册时,可同时备案一个备用培养基品种。
无血清培养基企业应抓住中国生物制药行业发展窗口期,在临床前就与生物制药企业合作开发无血清培养基配方,从而可以基本锁定临床及上市后C 无血清培养基业务,实现与生物制药行业共同成长。
品牌效应明显,市场进入壁垒高。全球GIBCO、JRH、Hyclone等三家占据无血清培养基大部分市场份额,拥有成熟的研发和客户体系。
业务稳定性强,适合并购整合。全球细胞培养基行业现有格局是通过多次并购整合形成的,尤其是Thermo Fisher,先并购Hyclone,在并购Life Technologies(旗下有GIBCO)后,又把Hyclone买给GE。
6. IVD上游试剂竞争格局

1)抗原抗体
Meridian Life Science公司成立于1977年,是一家生产多种抗体、病毒抗原、重组蛋白质,各类PCR多聚酶,各种核苷酸和重要体外诊断试剂的大型领军企业。同时也为生物制药和体外诊断企业提供研发,生产流程建立以及制造的外包合同服务,包括为I / II期的临床试验提供在cGMP规范下生产的各类生物制品。
美国Fitzgerald 公司是一家国际性知名抗体研发生产企业。Fitzgerald公司为全球试剂诊断公司与研究机构提供专业的抗体、纯化抗原以及工业诊断用大包装免疫原料。公司产品多达5000种,能够满足您对于最前沿科学研究的需求。产品涉及:单克隆抗体/抗原生育类、传染病类、TORCH系列、肿瘤标记物、心脏标记物、神经科学类、病毒类等。
Santa Cruz公司是全球最大的抗体生产厂商之一,目前公司提供二万余种研究用的第一抗体,几乎覆盖了目前生命科学研究的各个最新领域,其每种抗体又有多个克隆可以选择,还提供一些对应蛋白标准品及相关产品,如ABC试剂盒,各种标记二抗,Western试剂盒,蛋白分子量Marker,核抽提物等,为免疫学研究工作提供了极大的方便。
2)诊断酶
罗氏诊断致力于开发和提供从疾病的早期发现、预防到诊断、监测的创新、高性价比、及时和可靠的诊断系统和解决方案,从而帮助医务人员提高患者的治疗效果,改善人们生活质量,并减少社会医疗成本。罗氏集团拥有诊断和制药两个业务领域。
贝克曼是目前全球IVD领域中,设备、试剂、应用软件开发和制造最强的企业之一。其中IVD设备研发和销售是贝克曼最大的业务,其在全球范围内的实验室中大约有27万件仪器系统。贝克曼将其业务分为三大部门:临床诊断、生命科学和颗粒特性。
3)培养基
国际培养基包括GIBCO、JRH和HyClone,还有Irvine、LONZA、BD、Merck、LONZA和其它一些小众的培养基公司。
Thermo Fisher
Thermo Fisher细胞培养基业务是收购的,2009年收购美国犹他州Hyclone(成立于1960年代), 2013年收购Life Technologies(旗下GIBCO细胞培养基业务),又在2014年把Hyclone卖给了GEHealthcare。
GIBCO(Grand Island Biological Company)1960年代成立于美国纽约州,是Life Technologies旗下公司,Life Technologies在2000年被纳斯达克上市公司Invitrogen收购,Invitrogen在2009年再次并购Applied Biosystem,并更名为Life Technologies。
GIBCO主要产品包括化学成分界定的细胞培养基、无血清细胞培养基、基础细胞培养基及血清等产品。据了解,GIBCO年销售收入为10亿美元左右,为全球最大的细胞培养基供应商。
GE Healthcare
2014年GE Healthcare以10.6亿美元收购Thermo Fisher旗下的Hyclone的细胞培养、基因调控及磁珠三项业务,该业务2013年营业收入2.5亿美元左右。Hyclone成立于1967年,为基础研究开发高质量的胎牛血清,现有产品包括基础细胞培养基、无血清培养基、无蛋白培养基及一次性生物反应器等。
Merk
Merk在细胞培养基业务投入相当大,分别在2010年收购Millipore,2011年收购北京清大天一科技有限公司(清大天一主要业务在动物疫苗培养基。),2014年收购Sigma(旗下JRH细胞培养基公司)。2008年Sigma收购JRH Biosciences,年收入1.5亿美元左右,整合在旗下的SAFC Bioscience公司。
JRH Biosciences于1960年代成立于澳大利亚,主要产品包括基础培养基(DMEM、1640、MEM、M199)、无血清培养基(适用于CHO细胞、杂交瘤细胞、昆虫细胞等)和各种血清产品(澳大利亚及新西兰产地)。