近日,由北京阅微基因技术股份有限公司(下文简称“阅微基因”)自主研发的微卫星不稳定基因检测试剂盒(荧光PCR-毛细管电泳法)(下文简称“MSI试剂盒”或“本试剂盒”)正式获批国家药品监督管理局第三类医疗器械注册证(国械注准20213400936)。

本试剂盒是国内首款基于单核苷酸位点的微卫星不稳定检测试剂盒,通过荧光PCR+毛细管电泳法,可用于体外定性检测人结直肠癌福尔马林固定石蜡包埋组织切片样本中6个微卫星位点(BAT-25、BAT-26、NR-21、NR-24、NR-27、MONO-27)的不稳定状态,从而判断MSI分型状态,辅助诊断错配修复基因突变的结直肠癌。
示意图:微卫星不稳定基因检测试剂盒(荧光PCR-毛细管电泳法)
(国械注准20213400936)
注册临床试验严谨
本试剂盒的注册临床试验由中国医学科学院肿瘤医院牵头,复旦大学肿瘤医院和四川大学华西医院两家顶尖肿瘤医院共同参与,累计完成1000多例的临床样本验证。本试剂盒也是已上市产品中唯一与免疫组化进行对比研究的产品,符合FDA及NMPA的注册审批要求。
MSI临床应用广泛
微卫星(Microsatellite)是遍布于人类基因组中的短串联重复序列。大量研究表明,微卫星不稳定(Microsatellite Instability,MSI)由错配修复(MMR)基因发生缺陷引起,与肿瘤的发生密切相关。
林奇综合征是一种常染色体显性遗传肿瘤综合征,可引起结直肠及其他部位发生肿瘤,其风险高于正常人群。据报道90%林奇综合征具有MSI-H特征,国内外指南均明确指出MSI检测可用于林奇综合征初筛。
除此之外,MSI还在结直肠癌/胃癌/子宫内膜癌预后判断和化疗方案选择、PD-1/PD-L1免疫用药指导方面有重要的临床意义。截止目前MSI已经被写入了十多种癌种的NCCN指南中。
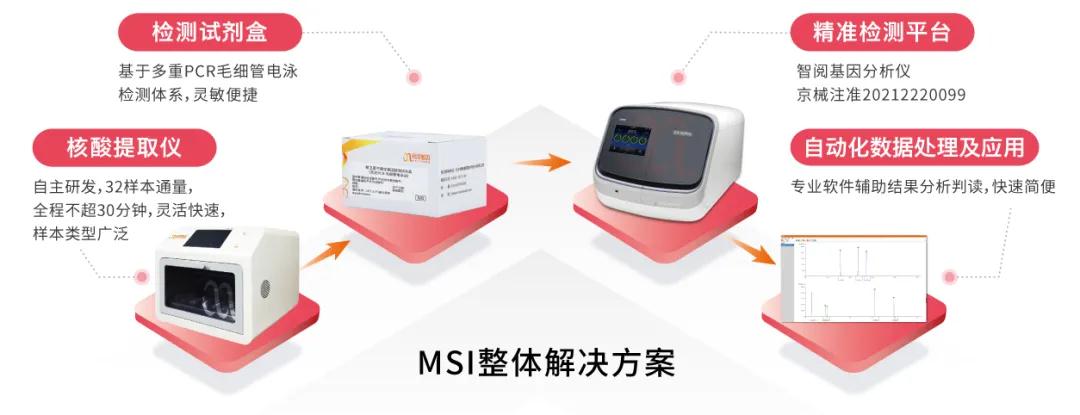
打造MSI整体解决方案
阅微基因基于临床病理检测工作中涉及到的核酸提取、扩增检测、报告分析全流程推出的MSI整体解决方案,解决了MSI检测操作繁琐、判读困难、报告周期长等临床痛点,可更准确、高效地辅助临床决策,造福更多肿瘤患者。
 阅微基因自2011年获得国内首个MSI复合扩增体系专利(专利号 : ZL 2011 1 0152226. X)以来,一直潜心致力于MSI产品研发,期望为社会和临床精准诊疗提供优异的产品。十年磨一剑,阅微基因MSI试剂盒此次获批受到了社会各界的关注和帮助,在经历大量临床样本的严谨验证、注册生产体系的严格审核后,终于获批上市。未来阅微基因将继续深入MSI及分子病理的探索和研发,为临床精准诊疗提供更有利武器。
阅微基因自2011年获得国内首个MSI复合扩增体系专利(专利号 : ZL 2011 1 0152226. X)以来,一直潜心致力于MSI产品研发,期望为社会和临床精准诊疗提供优异的产品。十年磨一剑,阅微基因MSI试剂盒此次获批受到了社会各界的关注和帮助,在经历大量临床样本的严谨验证、注册生产体系的严格审核后,终于获批上市。未来阅微基因将继续深入MSI及分子病理的探索和研发,为临床精准诊疗提供更有利武器。

阅微基因于2009年正式运营,是一家集体外诊断产品研发、生产、经营于一体的生命科学机构。阅微基因致力于基因检测技术的产品化,专注于基因检测“金标准”,基于毛细管电泳技术平台,通过原创性多重荧光扩增技术的革新,研发出一系列准确、快速、简便、经济的检测试剂及仪器,应用于临床、法医和工业领域。
阅微基因总部位于北京市海淀区中关村科技园区,在北京和苏州两地设有GMP生产基地,并在全国设有多个技术服务中心,及时响应客户需求。2018年阅微基因在哈萨克斯坦成立海外子公司,开始积极拓展海外业务。
阅微基因获得了数十项发明专利及软件著作权,并在快速基因检测方面取得了优异的成绩。经过多年的努力,阅微基因已成为基因检测行业的一家高知名度公司,match并与中国和世界的研究机构合作。阅微基因自行开发的产品设计用于各种应用,包括肿瘤伴随诊断、生殖遗传、精准用药、法庭科学DNA鉴定及工业领域等。
声明:转载此文是出于传递更多信息之目的。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。