来源: 药明康德2022年06月22日 10:53
神经系统疾病正在成为全球最大的疾病负担之一,且随着老龄化加剧愈演愈烈。在日前结束的药明康德健康产业论坛上,参与专题讨论的专家预测,神经系统疾病领域是产业未来的风口。过去十年中,使用基因疗法在中枢神经系统疾病治疗方面取得了很大的进展。中枢神经系统疾病对患者的生理及心理健康存在着严重的威胁,同时因其致病机制较复杂,因此存在着许多未被满足的治疗需求。许多单基因突变导致疾病的突变已经被确定,疗法已被开发,如治疗脊髓性肌萎缩的诺健生(Zolgensma)通过递送正常SMN1基因进行治疗,已在2019年上市。随着对某些非单基因疾病发病机制的不断加深理解,新的基因治疗方式不断涌现。
内容概要 2022年临床积极进展
注:本文讨论基因疗法指在患者体内通过递送转基因来治疗疾病的疗法,不包含体外基因疗法(使用基因工程改造细胞再输回体内)、细胞疗法、寡核苷酸疗法。
2022年临床积极进展 未来一年内重要里程碑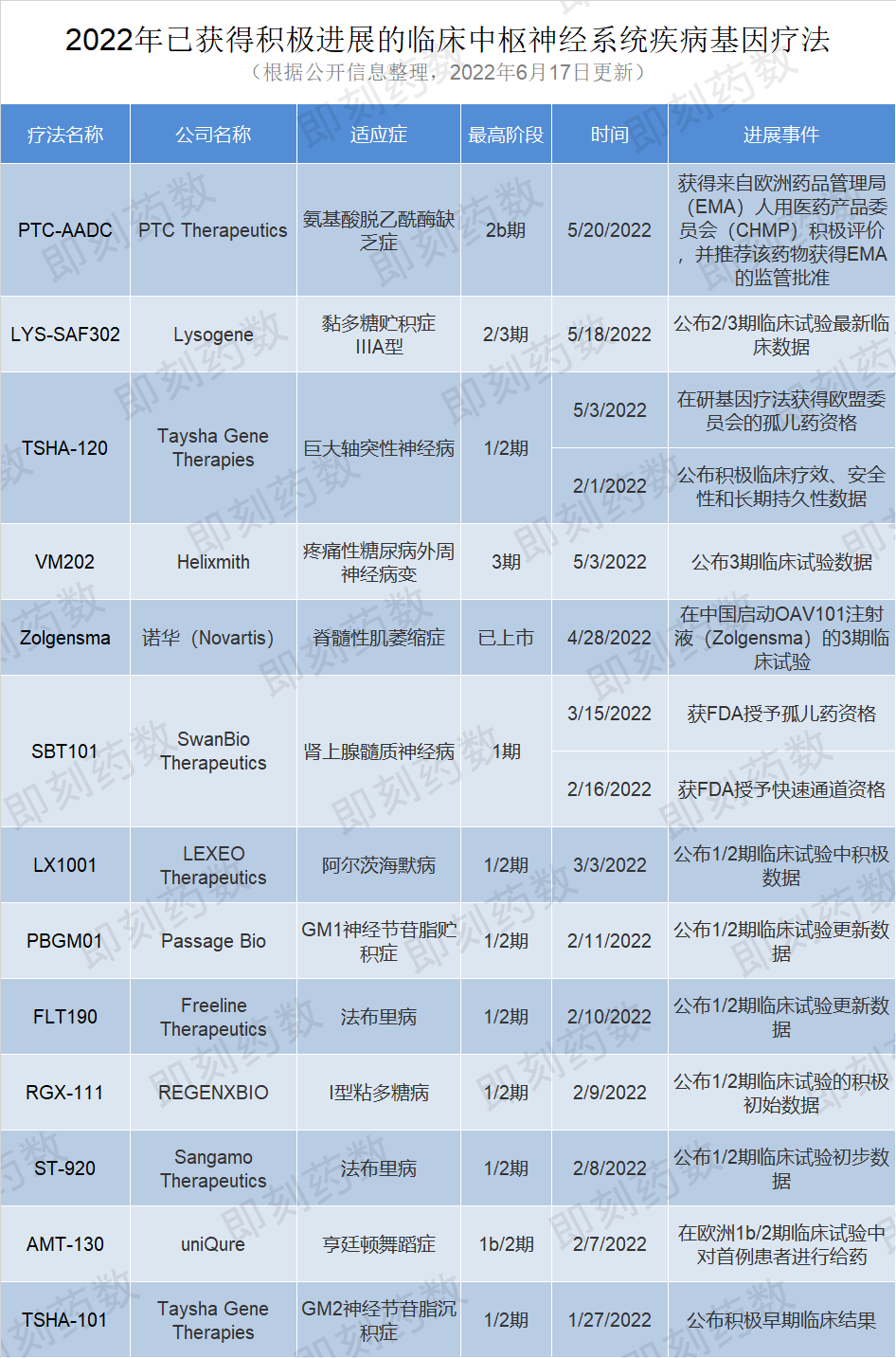
公司名称: PTC Therapeutics
适应症: 氨基酸脱乙酰酶缺乏症(AADC)

药物名称:LYS-SAF-302
公司名称:Lysogene
适应症:粘多糖贮积症ⅢA型

药物名称:VM202(donaperminogene seltoplasmid)
公司名称:Helixmith
适应症:糖尿病性神经病(DPN)

VM202(donaperminogene seltoplasmid)是一种潜在“first-in-class”非病毒的质粒DNA基因疗法。用于治疗糖尿病性神经病(DPN)的3期临床研究分多个部分进行,一部分为期9个月(VMDN-003;500名受试者),另一部分延长3个月至12个月(VMDN-003b;101名受试者)。Helixmith在美国启动了DPN的第二部分3期试验VMDN-003-2,目标是在2022年底之前发布顶线结果。该公司计划在2022年下半年启动临床3期试验的第3部分。
其余有望达到1期或2期临床开发里程碑的中枢神经系统基因疗法请见下图。
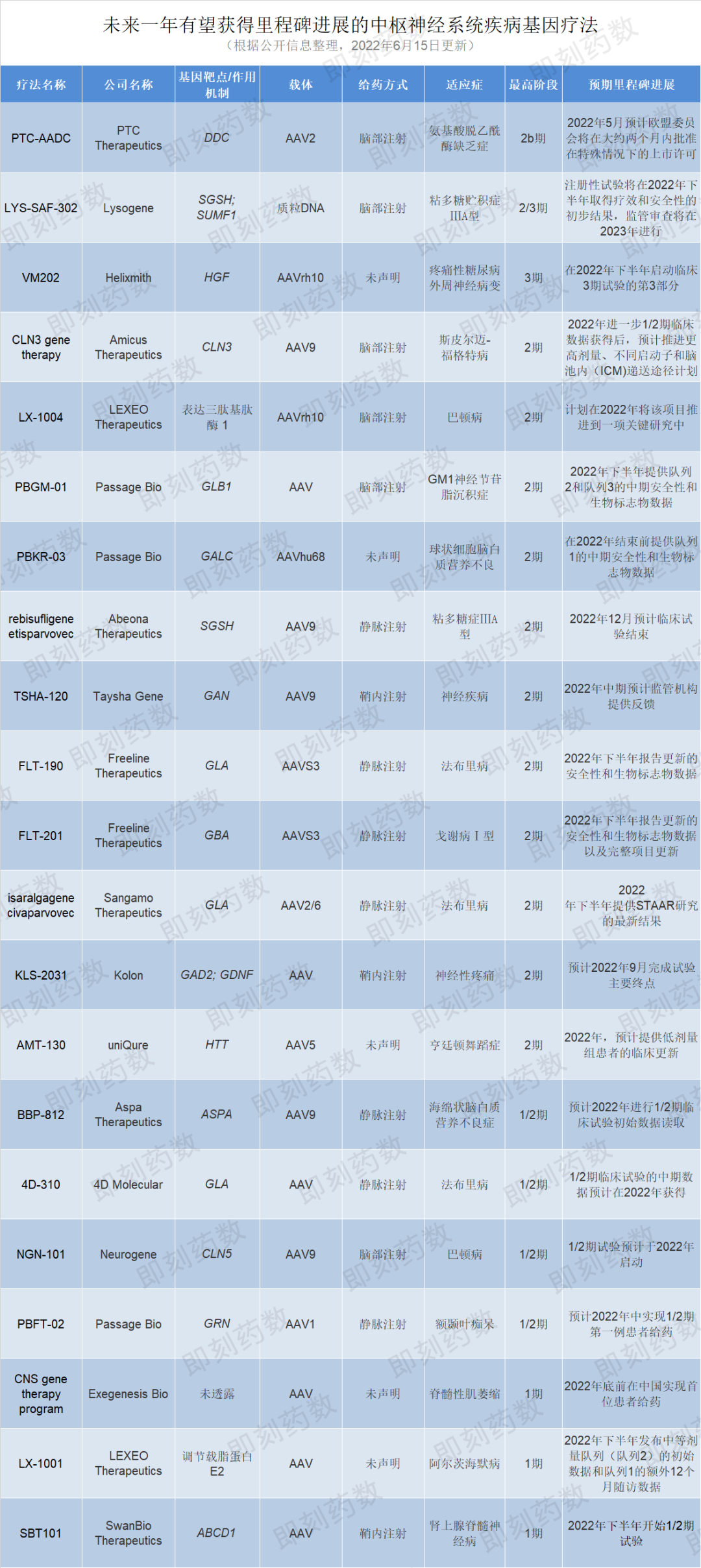
▲未来一年有望获得里程碑进展的中枢神经系统疾病基因疗法(图片来源:药明康德内容团队制图)
未来十年潜在发展方向 1 适应症患者群体扩大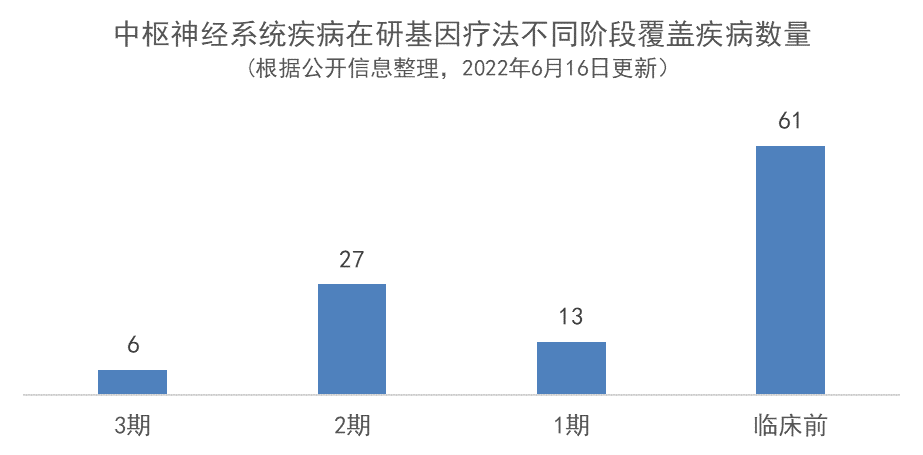
在中枢神经系统疾病已经进行至中后期临床试验的基因疗法中,覆盖的疾病范围多为单基因变异导致的神经系统罕见遗传疾病,如氨基酸脱乙酰酶缺乏症、粘多糖贮积症ⅢA型、脊髓型肌萎缩、法布里病等。基因疗法主要通过对单基因进行调节,有望对这些疾病进行“一次性治疗”效果。
2 递送载体中AAV9为主流,此基础上不断开发 3 蛋白表达类基因疗法的比例上升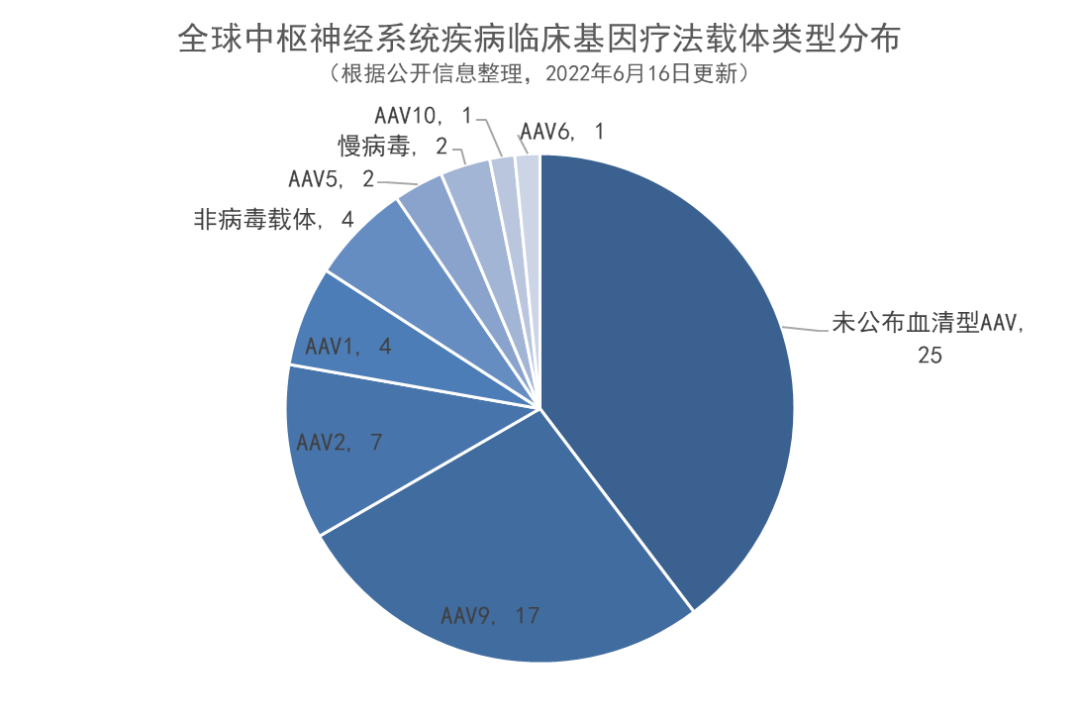
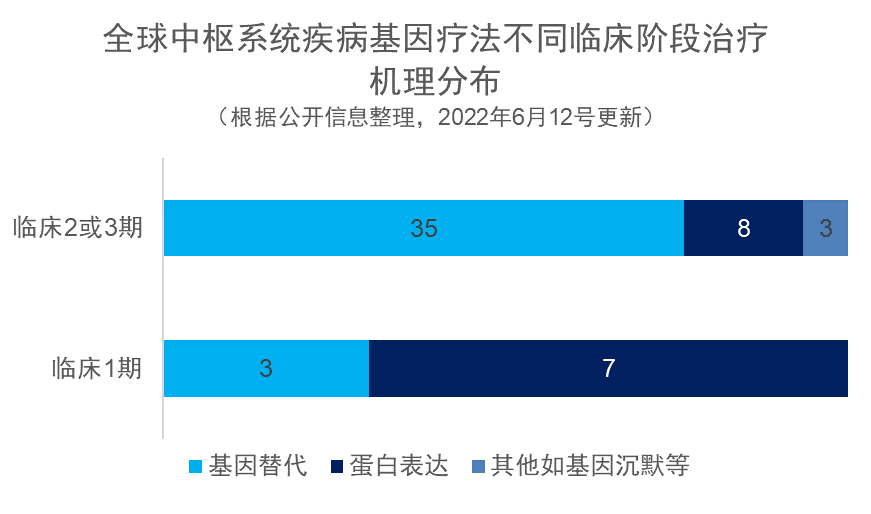
4 3种给药技术、创新辅助技术被开发
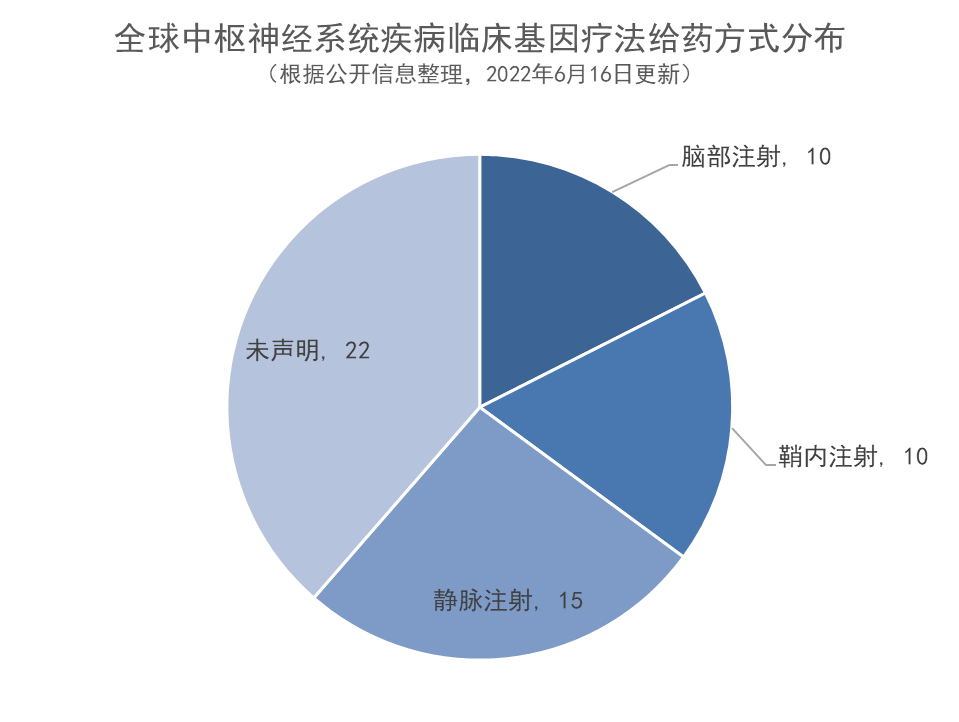
参考文献:
[1] Lysogene Provides Clinical Update on AAVance Phase 2/3 Clinical Trial with Gene Therapy LYS-SAF302 for the Treatment of MPS IIIA at the 25th Annual ASGCT Meeting. Retrieved 2022-05-19, from https://www.businesswire.com/news/home/20220517005897/en
[2] Taysha Gene Therapies Receives Orphan Drug Designation from the European Commission for TSHA-120 for the Treatment of Giant Axon Neuropathy (GAN). Retrieved 2022-05-04, from https://www.globenewswire.com/news-release/2022/05/03/2434345/0/en/Taysha-Gene-Therapies-Receives-Orphan-Drug-Designation-from-the-European-Commission-for-TSHA-120-for-the-Treatment-of-Giant-Axon-Neuropathy-GAN.html
[3] Taysha Gene Therapies Reports Positive Clinical Efficacy and Safety Data for High Dose Cohort and Long-term Durability Data for TSHA-120 in Giant Axonal Neuropathy. Retrieved 2022-02-01, from https://www.businesswire.com/news/home/20220131005317/en
[4] Helixmith Announces VM202 (Engensis®) Presentation at New York Academy of Sciences "Advances in Pain" Meeting on May 3, 2022. Retrieved 2022-05-03, from https://www.prnewswire.com/news-releases/helixmith-announces-vm202-engensis-presentation-at-new-york-academy-of-sciences-advances-in-pain-meeting-on-may-3-2022-301536808.html
[7] FDA Grants Orphan Drug Designation to SBT101, the First Investigational AAV-Based Gene Therapy for Adrenomyeloneuropathy (AMN). Retrieved 2022-03-16, from https://www.businesswire.com/news/home/20220315005309/en
[9] Freeline Presents on Its Fabry and Gaucher Disease AAV-Based Gene Therapies at the 18th Annual WORLDSymposium™. Retrieved 2022-02-10, from https://www.biospace.com/article/releases/freeline-presents-on-its-fabry-and-gaucher-disease-aav-based-gene-therapies-at-the-18th-annual-worldsymposium-/
[10] Sangamo Therapeutics Announces Updated Preliminary Phase 1/2 Data Showing Tolerability and Sustained Elevated α-Gal A Enzyme Activity in Patients With Fabry Disease. Retrieved 2022-02-08, from https://www.businesswire.com/news/home/20220207005059/en
[11] PTC Therapeutics Receives Positive CHMP Opinion for Upstaza™ for the Treatment of AADC Deficiency. Retrieved June 15, 2022, from https://www.prnewswire.com/news-releases/ptc-therapeutics-receives-positive-chmp-opinion-for-upstaza-for-the-treatment-of-aadc-deficiency-301551996.html
[12] Corporate Presentation. Retrieved June 15, 2022, from https://www.lysogene.com/wp-content/uploads/2022/04/Lysogene-Corporate-Presentation-Jan31.pdf
[13] LEXEO THERAPEUTICS ANNOUNCES POSITIVE INITIAL DATA FROM ONGOING PHASE 1/2 CLINICAL TRIAL OF AAV-BASED GENE THERAPY CANDIDATE LX1001 IN PATIENTS WITH ALZHEIMER’S DISEASE. Retrieved June 16, 2022, from https://www.lexeotx.com/post/lexeo-therapeutics-announces-positive-initial-data-from-ongoing-phase-1-2-clinical-trial-of-aav-based-gene-therapy-candidate-lx1001-in-patients-with-alzheimers-disease/
[14] Goertsen, et al., (2019). AAV capsid variants with brain-wide transgene expression and decreased liver targeting after intravenous delivery in mouse and marmoset. Nature Neuroscience. https://doi.org/10.1038/s41593-021-00969-4
本文著作权属原创者所有,不代表本站立场。我们转载此文出于传播更多资讯之目的,如涉著作权事宜请联系删除。